Eigenschaften/WirkungenATC-Code
D05AX52
Wirkungsmechanismus
Enstilar Schaum kombiniert die pharmakologischen Wirkungen von Calcipotriol-Monohydrat als synthetisches Vitamin D3 Derivat und Betamethasondipropionat als synthetisches Kortikosteroid.
Wie andere topische Kortikosteroide hat Betamethasondipropionat in Enstilar entzündungshemmende, immunsuppressive und vasokonstriktorische Eigenschaften. In Kombination haben Calcipotriol und Betamethasondipropionat in Enstilar grössere entzündungshemmende und anti-proliferative Wirkungen als jede Komponente allein. Doch während ihre pharmakologischen und klinischen Effekte bekannt sind, ist ihr genauer Wirkmechanismus in Psoriasis vulgaris nicht vollständig geklärt.
Pharmakodynamik
Vasokonstriktion:
In einer Studie zur Vasokonstriktion in gesunden Probanden wurde Enstilar mit Kortikosteroiden verschiedener Stärkeklassen verglichen und die vasokonstriktorische Antwort von Enstilar war signifikant grösser als diejenige einer Calcipotriol- und Betamethasondipropionat-haltigen Salbe (klassifiziert als wirksames Kortikosteorid, Klasse III), aber kleiner als diejenige einer Clobetasol-haltigen Creme (hochwirksames Kortikosteorid, Klasse IV).
Unterdrückung der Hypothalamus-Hypophysen-Nebennieren-Achse:
Kurzzeitdaten über 4 Wochen
Unter Bedingungen mit maximaler Anwendung, bei Probanden mit ausgedehnter Psoriasis auf dem Körper und der Kopfhaut, welche bis zu 4 Wochen behandelt wurden, wurde die adrenale Antwort auf ACTH (adrenocorticotropes Hormon) durch eine Messung des Kortisol-Levels bestimmt. Keiner der 35 Probanden hatte 30-60 Minuten nach ACTH Stimulation erniedrigte Kortisolwerte im Blutserum.
Langzeitdaten
Die adrenale Antwort auf ACTH wurde in einer Untergruppe bei erwachsenen Probanden mit mittelschwerer bis schwerer Psoriasis vulgaris bewertet, bei denen mindestens 10 % der Körperoberfläche betroffen waren. Die Probanden wurden randomisiert und erhielten zweimal wöchentlich bis zu 52 Wochen lang Enstilar oder Vehikelschaum (Langzeit-Erhaltungsbehandlung). Patienten mit Rezidiv wurden 4 Wochen lang 1x täglich mit Enstilar behandelt und anschliessend randomisiert weiterbehandelt.
Nach 52 Wochen Behandlung hatten insgesamt 2 von 21 Probanden in der Enstilar-Gruppe und 1 von 19 Probanden in der Vehikelschaumgruppe 30 Minuten nach der ACTH-Exposition Kortisolspiegel ≤18 µg/dl. Ein 3. Proband im Enstilar Arm, der nach 30 Minuten einen normalen Cortisol Wert hatte, zeigte einen verminderten Cortisol Wert ≤18 µg/dL nach 60 Minuten. Keiner der Probanden in einer der Behandlungsgruppen hatte nach sowohl 30 als auch nach 60 Minuten Kortisolspiegel ≤18 µg/dl (siehe «Warnhinweise und Vorsichtsmassnahmen»). In dieser Studie wurden keine klinisch relevanten Auswirkungen auf den Kalziummetabolismus festgestellt.
Effekte auf den Kalziummetabolismus:
Auswirkungen auf den Kalziummetabolismus einer einmal täglichen Anwendung von Enstilar während 4 Wochen in erwachsenen Probanden (N = 564) mit Psoriasis vulgaris wurden auch in drei randomisierten, multizentrischen, prospektiven Vehikel- und/oder aktiv kontrollierten klinischen Studien untersucht. Nach einmaliger täglicher Anwendung von Enstilar wurden erhöhte Serum-Kalziumspiegel ausserhalb des normalen Bereichs in 3 Probanden beobachtet. Erhöhte Kalziumspiegel im Spontanurin ausserhalb des normalen Bereichs wurden bei 17 Patienten beobachtet.
Enstilar Schaum verursachte in diesen Studien wiederholt eine höhere mittlere Kalzium im Urin/Kreatinin Ratio als die Vergleichsbehandlungen mit Daivobet® Salbe. Dies ist ein Hinweis, dass Enstilar Schaum einen stärkeren katabolen Effekt auf den Knochenstoffwechsel zeigt als Daivobet® Salbe. Der Effekt von Enstilar Schaum auf den Knochenstoffwechsel wurde maximal über 4 Wochen untersucht. Eine längere Behandlung mit Enstilar Schaum wird nicht empfohlen.
Klinische Wirksamkeit
Kurzzeitdaten über 4 Wochen
Die klinische Wirksamkeit Enstilar der einmal täglichen Anwendung wurde in drei randomisierten Doppelblindstudien während 4 Wochen untersucht, mit über 1100 Patienten mit Psoriasis auf dem Körper (Kopfhaut in Studie 2 eingeschlossen), mit mindestens leichtem Schweregrad gemäss Physician's Global Assesment of desease severity (PGA), mit mindestens 2% der betroffenen Körperoberfläche (BSA; body surface area) und mit einem m-PASI Wert (modified psoriasis area severity index) von mindestens 2. Die Bestimmung des Schwergrads der Psoriasis (PGA) wird, basierend auf der durchschnittlichen psoriatischen Läsion, mittels einer 5-Stufen Skala (keine, fast keine, leichte, mittelschwere, schwere) gemacht. Der m-PASI Wert ist eine zusammengesetzte Punktezahl, welche den Schweregrad (Hautrötung, Schuppung, Verhärtung) und die betroffene Körperregion (Gesicht und Hautfalten ausgeschlossen) beschreibt.
In Studie 1 wurden 426 Patienten zufällig entweder der Gruppe «Enstilar Schaum» oder der Gruppe «Vehikelschaum» zugeteilt. In Studie 2, wurden 302 Patienten zufällig entweder der Gruppe «Enstilar Schaum», «Betamethasondipropionate (BDP) in Vehikelschaum» oder «Calcipotriol in Vehikelschaum» zugeteilt. In Studie 3 wurden 376 Patienten zufällig entweder der Gruppe «Enstilar Schaum», «Daivobet Salbe», «Vehikelschaum» oder «Vehikelsalbe» zugeteilt. Der primäre Endpunkt war Patienten mit «Behandlungserfolg» («keine», oder «fast keine» bei Patienten mit mindestens «mittelschwerere» Erkrankung zu Beginn der Behandlung (Basis), «keine» für Patienten mit leichter Erkrankung zu Beginn der Behandlung) gemäss PGA nach Woche 4.
Krankheitsbezogene Basischarakteristika
|
|
Studie 1 (N=426)
|
Studie 2 (N=302)
|
Studie 3 (N=376)
| |
Basis Schweregrad (PGA)
| |
Leicht
|
65 (15,3%)
|
41 (13,6%)
|
63 (16,8%)
| |
Mittelschwer
|
319 (74,9%)
|
230 (76,2%)
|
292 (77,7%)
| |
Schwer
|
42 (9,9%)
|
31 (10,3%)
|
21 (5,6%)
| |
Ø Körperoberfläche (Bereich)
|
7,5% (2 – 30%)
|
7,1% (2 – 28%)
|
7,5% (2 - 30%)
| |
Ø m-PASI (Bereich)
|
7,5 (2,0 - 47,0)
|
7,6 (2,0 - 28,0)
|
6,8 (2,0 - 22,6)
|
Anteil Patienten mit «Behandlungserfolg» gemäss PGA nach Woche 4
|
|
Enstilar
|
Vehikelschaum
|
BDP in Vehikelschaum
|
Calcipotriol Vehikelschaum
|
Daivobet® Salbe
|
Vehikelsalbe
| |
Studie 1
|
(N=323)
53,3%
|
(N=103)
4,8%
|
-
|
-
|
-
|
-
| |
Studie 2
|
(N=100)
45,0%
|
-
|
(N=101)
30,7%
|
(N=101)
14,9%
|
-
|
-
| |
Studie 3
|
(N=141)
54,6%
|
(N=49)
6,1%
|
-
|
-
|
(N=135)
43,0%
|
(N=51)
7,8%
|
Die Ergebnisse des primären Endpunkts «Behandlungserfolg» (PGA) am Körper nach 4 Wochen zeigten, dass Enstilar signifikant stärker wirksam als alle in die Studie einbezogenen Vergleichssubstanzen war. Ein Ansprechen wurde in allen Kategorien der Erfassung des Ausgangsschweregrads der Erkrankung beobachtet.
Die Lebensqualität wurde in Studie 1 mittels des generischen EQ-5D-5L und des dermatologischen DLQI untersucht. Ab 1 Woche über die gesamte Behandlungsphase hinweg wurden bei den Patienten, die Enstilar erhielten, grössere Verbesserungen der mittels DLQI gemessenen Lebensqualität als bei den Patienten, die Vehikelschaum erhielten, gezeigt. Nach 4 Wochen wurde eine signifikant grössere Verbesserung der mittels EQ-5D-5L gemessenen Lebensqualität zugunsten der Patienten, die Enstilar erhielten, im Vergleich zu den Patienten, die Vehikelschaum erhielten, gezeigt.
Langzeitdaten
In der randomisierten, doppelblinden, Vehikel kontrollierten Studie LP0053-1004 (NCT02899962) wurde die Langzeitanwendung von Enstilar Schaum bei Patienten mit Psoriasis bewertet, die einen anhaltenden Behandlungserfolg erzielten (definiert als ein Physician's Global Assesment of disease severity (PGA) Score von «keine» oder «fast keine» mit mindestens 2 Stufen Verbesserung vom Ausgangswert). Initial wurden insgesamt 650 Patienten mit Psoriasis in einer offenen 4-wöchigen Behandlung (run-in Phase) mit einmal täglichem Enstilar Schaum therapiert. Von den Patienten, die nach den 4 Wochen das Therapieziel unter Enstilar Schaum erreichten, wurden 521 Patienten randomisiert, um zweimal wöchentlich an 2 nicht aufeinander folgenden Tagen weiter Enstilar Schaum oder Vehikel Schaum für insgesamt 52 zusätzliche Wochen zu erhalten. Der Schweregrad der Psoriasis wurde unter Verwendung eines 5-Punkte-PGA Scores bewertet. Die Mehrheit der Patienten in dieser Studie (82%) hatte zu Studienbeginn eine Erkrankung mit «mittelschwerem» Schweregrad, 11% der Patienten hatten zu Studienbeginn eine Erkrankung mit «leichtem» Schweregrad und 7% der Patienten hatten zu Studienbeginn eine «schwere» Erkrankung. Das Ausmass der Krankheitsbeteiligung, gemessen an der mittleren Körperoberfläche, betrug zu Studienbeginn 8,3% (Bereich 1 bis 38%). Patienten aus beiden Armen, bei denen während der 52 Wochen ein Ansprechverlust auftrat (definiert als ein PGA-Wert von mindestens «leicht»), wurden 4 Wochen lang einmal täglich mit Enstilar Schaum behandelt. Anschliessend wurden diejenigen, die nach 4 Wochen täglicher Therapie mit Enstilar Schaum wieder einen PGA-Wert von «keine» oder «fast keine» erreichten, mit der ursprünglich randomisierten Behandlung mit Enstilar Schaum bzw. Vehikel Schaum an 2 Tagen pro Woche weitertherapiert.
Die mediane Zeit bis zum Verlust der therapeutischen Wirkung betrug 56 Tage für Patienten, die zweimal wöchentlich mit Enstilar Schaum behandelt wurden, verglichen mit 30 Tagen für Patienten, die zweimal wöchentlich mit Vehikel Schaum behandelt wurden. Während des 52-wöchigen Beurteilungszeitraums traten bei Patienten in der Gruppe mit zweimal wöchentlichem Enstilar Schaum median 2,0 Rezidive auf, im Vergleich zu Patienten in der Gruppe mit zweimal wöchentlichem Vehikel Schaum mit median 3,0 Rezidiven über 52 Wochen.
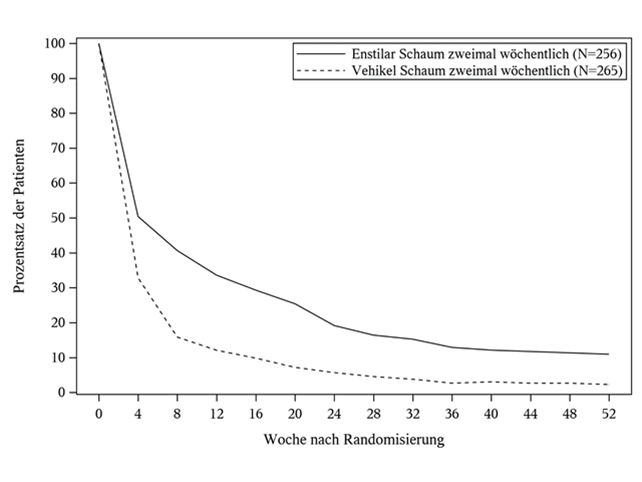
Die verfügbaren Daten zum Verbrauch bei der Rescue Therapie zeigten keinen konsistenten Vorteil von Enstilar im Vergleich zur Vehikel. Es kann nicht ausgeschlossen werden, dass bei einer Untergruppe der dauerhaft mit Enstilar therapierten Personen der Verbrauch von Enstilar stark zunimmt. Abbildung 1 zeigt den Prozentsatz der Probanden, die bis Woche 52 nach der Randomisierung einen PGA-Wert von «keine» oder «fast keine» beibehalten.
Abbildung 1: Prozentsatz der Patienten, die bis Woche 52 nach der Randomisierung einen PGA-Wert von «keine» oder «fast keine» beibehalten haben
|

