Eigenschaften/WirkungenATC-Code
L01EH02
Wirkungsmechanismus
Neratinib bindet an den HER2-Rezeptor, verringert die EGFR- und HER2-Autophosphorylierung der nachgelagerten MAPK- und AKT-Signalpfade und hemmt wirksam die Tumorzellproliferation in vitro. Neratinib hemmte EGFR- und/oder HER2-exprimierende Karzinomzelllinien mit einer zellulären IC50 <100 nM.
Pharmakodynamik
Neratinib ist ein irreversibler Tyrosinkinasehemmer (TKI) des viralen Onkogen-Homologs der Erythroblastenleukämie (ERBB), der die Signaltransduktion des mitogenen Wachstumsfaktors durch kovalente Bindung mit hoher Affinität an der ATP-Bindungsstelle von 3 epidermalen Wachstumsfaktorrezeptoren (EGFRs) blockiert: EGFR (codiert als ERBB1), HER2 (codiert als ERBB2) und HER4 (codiert als ERBB4) oder ihre aktiven Heterodimere mit HER3 (codiert als ERBB3). Dadurch wird eine nachhaltige Hemmung dieser wachstumsfördernden Pfade bei Brustkrebs mit HER2-Amplifizierung oder -Überexpression oder HER2-Mutation erreicht.
Klinische Wirksamkeit
In der multizentrischen, randomisierten, doppelblinden, placebokontrollierten Phase-III-Pivotstudie ExteNET (3004) wurden 2.840 Frauen mit HER2-positivem Brustkrebs (lokal bestätigt durch Laboruntersuchung) im Frühstadium, die eine adjuvante Behandlung mit Trastuzumab und eine Chemotherapie abgeschlossen hatten, 1:1 randomisiert und erhielten ein Jahr lang täglich entweder Nerlynx oder ein Placebo. Das mediane Alter in der zu behandelnden (ITT) Population betrug 52 Jahre (59,9% waren ≥50 Jahre alt, 12,3% waren ≥65 Jahre alt); 81,0% waren kaukasische Patientinnen, 2,6% waren schwarze oder afroamerikanische Patientinnen, 13,6% waren asiatische Patientinnen und 2,9% wiesen eine sonstige ethnische Zugehörigkeit auf. Zum Baseline-Zeitpunkt hatten 57,4% eine Hormonrezeptor-positive Erkrankung (definiert als ER-positiv und/oder PgR-positiv), 23,6% wiesen keine Lymphknotenmetastasen auf, 46,8% hatten einen bis drei positive Lymphknoten und 29,6% hatten vier oder mehr positive Lymphknoten. Etwa 10% der Patientinnen hatten Stadium-I-Tumore, etwa 40% hatten Stadium-II-Tumore und etwa 30% hatten Stadium-III-Tumore. Der Median für den Zeitraum von der letzten adjuvanten Trastuzumab-Behandlung bis zur Randomisierung lag bei 4,5 Monaten.
Der primäre Wirksamkeitsendpunkt der Studie war das Überleben frei von invasiver Erkrankung (invasive disease-free survival, iDFS). Die sekundären Wirksamkeitsendpunkte der Studie umfassten das krankheitsfreie Überleben (disease-free survival, DFS), einschliesslich duktalem Karzinom in situ (DFS-DCIS), die Zeit bis zum Auftreten von Fernmetastasen (time to distant recurrence, TTDR), das Überleben frei von Fernmetastasen (distant disease-free survival, DDFS), die kumulative Inzidenz von Rezidiven im Zentralnervensystem und das Gesamtüberleben (overall survival, OS).
Die primäre Analyse der Studie 2 Jahre nach der Randomisierung zeigte, dass Nerlynx in der ITT-Population das Risiko für Wiederauftreten einer invasiven Erkrankung oder Tod um 34% (RR = 0,66 mit 95-%-KI (0,49, 0,90), zweiseitiges p = 0,008) verringerte.
Tabelle 6: Primäre Wirksamkeitsanalysen – ITT- und Hormonrezeptor-positive Populationen, bei denen der Abschluss der Trastuzumab- und Chemotherapie weniger als ein Jahr zurücklag
|
Variable
|
Geschätzte Raten für 2-jährige Ereignisfreiheit1
(%)
|
Relatives Risiko
(95-%-KI)2
|
p-Wert3
| |
|
ITT-Population
| |
|
Nerlynx
(N = 1.420)
|
Placebo
(N = 1.420)
|
|
| |
Überleben ohne invasive Erkrankung
|
94,2
|
91,9
|
0,66
(0,49; 0,90)
|
0,008
| |
Krankheitsfreies Überleben, einschliesslich duktales In-situ-Karzinom
|
94,2
|
91,3
|
0,61
(0,45; 0,83)
|
0,001
| |
Überleben ohne Fernmetastasen
|
95,3
|
94,0
|
0,74
(0,52; 1,05)
|
0,094
| |
Zeit bis zum Auftreten von Fernmetastasen
|
95,5
|
94,2
|
0,73
(0,51; 1,04)
|
0,087
| |
ZNS-Rezidiv
|
0,92
|
1,16
|
–
|
0,548
| |
|
Hormonrezeptor-positive Population, bei der der Abschluss der Trastuzumab-Therapie weniger als ein Jahr zurücklag
| |
|
Nerlynx
(N = 670)
|
Placebo
(N = 664)
|
Relatives Risiko
(95-%-KI)4
|
p-Wert5
| |
Überleben ohne invasive Erkrankung
|
95,3
|
90,8
|
0,49
(0,30; 0,78)
|
0,002
| |
Krankheitsfreies Überleben, einschliesslich duktales In-situ-Karzinom
|
95,3
|
90,0
|
0,45
(0,28; 0,71)
|
<0,001
| |
Überleben ohne Fernmetastasen
|
96,1
|
92,9
|
0,53
(0,31; 0,88)
|
0,015
| |
Zeit bis zum Auftreten von Fernmetastasen
|
96,3
|
93,3
|
0,53
(0,30; 0,89)
|
0,017
| |
ZNS-Rezidiv
|
0,34
|
1,01
|
–
|
0,187
|
ZNS = Zentralnervensystem
1 Ereignisfreie Raten für alle Endpunkte mit Ausnahme von ZNS-Rezidiven, da in diesem Fall die kumulative Inzidenz berichtet wird.
2 Stratifiziertes proportionales Hazard-Modell nach Cox.
3 Stratifizierter, zweiseitiger Log-Rank-Test für alle Endpunkte mit Ausnahme von ZNS-Rezidiven, da in diesem Fall die Gray-Methode verwendet wurde.
4 Nicht stratifiziertes proportionales Hazard-Modell nach Cox.
5 Nicht stratifizierter, zweiseitiger Log-Rank-Test für alle Endpunkte mit Ausnahme von ZNS-Rezidiven, da in diesem Fall die Gray-Methode verwendet wurde.
Abbildung 1: Kaplan-Meier-Grafik für krankheitsfreies Überleben – Hormonrezeptor-positive Population, bei der der Abschluss der Trastuzumab- und Chemotherapie weniger als ein Jahr zurücklag
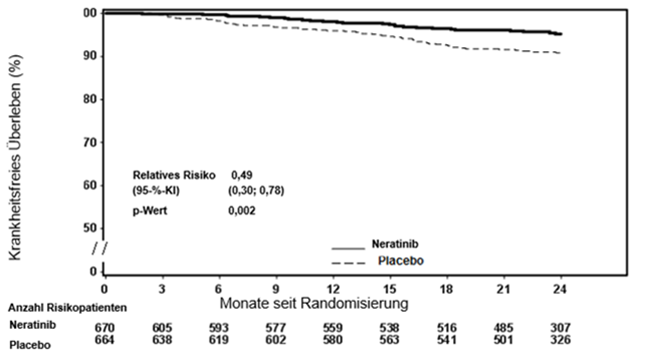
Etwa 75% der Patienten willigten in eine über 24 Monate hinausgehende Nachuntersuchung ein. Beobachtungen mit fehlenden Daten wurden zum Datum der letzten Untersuchung zensiert. Der Nutzen der Behandlung mit Nerlynx gegenüber Placebo blieb nach fünf Jahren bestehen, die Effektgrösse kann jedoch nicht zuverlässig abgeschätzt werden.
Bei Hormonrezeptor-negativen Patienten betrug das relative Risiko für iDFS nach 2 Jahren unabhängig von der Zeit seit der Trastuzumab-Therapie 0,93 mit einem 95-%-KI von 0,60 bis 1,43. In dieser Population wurde die Wirksamkeit nicht nachgewiesen.
An der Pivotstudie 3004 haben ausschliesslich Patientinnen teilgenommen, die zuvor mit Trastuzumab und Chemotherapie behandelt wurden.
Der relative Nutzen der Behandlung mit Nerlynx für hormonrezeptor-positive Patienten innerhalb von im Voraus festgelegten Patientenuntergruppen wird in Abbildung 2 dargestellt.
Bei der Betrachtung der nachstehenden Grafiken ist das absolute Rezidivrisiko zu berücksichtigen, wenn das Risiko/Nutzen-Verhältnis und somit der Nutzen einer Nerlynx-Therapie für die jeweilige Patienten-Untergruppe beurteilt wird. Bei diesen Analysen nach Patienten-Untergruppen ist die Anzahl der Rezidivereignisse in der jeweiligen Untergruppe zu beachten, nicht nur die relative Reduktion des Rezidivrisikos, um den Nutzen zu beurteilen, den die Patienten aus einer Behandlung mit Nerlynx ziehen könnten.
Abbildung 2: Hormonrezeptor-positive Patienten, krankheitsfreies Überleben nach Patientenuntergruppe
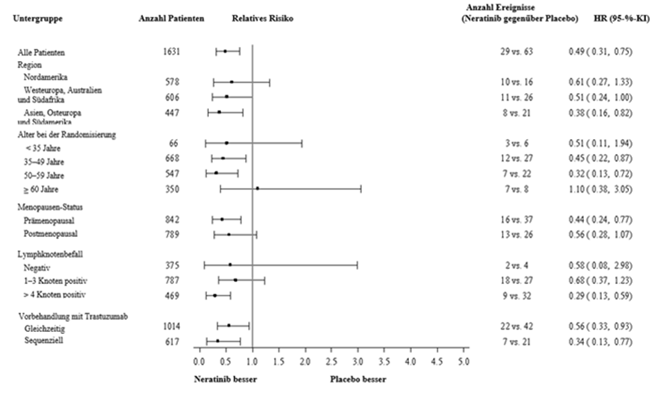
Abbildung 3: Hormonrezeptor-positive Patientinnen, krankheitsfreies Überleben nach Patientenuntergruppe (weitere Untergruppen
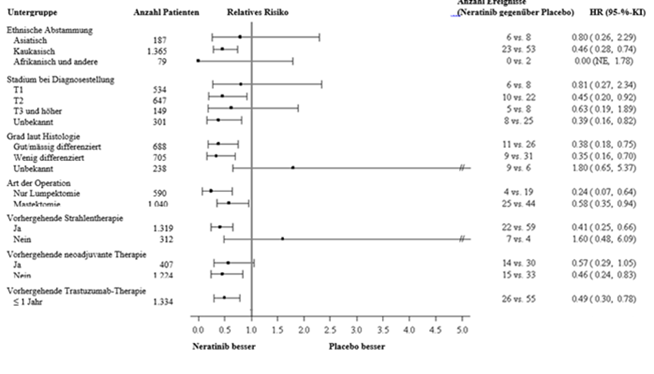
Bei einem medianen Follow-up von 8,06 Jahren gab es in der ITT-Population keinen statistisch signifikanten Unterschied im OS zwischen dem Nerlynx- und dem Placebo-Arm [HR 0,96 (95% CI: 0,75, 1,22)].
Ein den Nerlynx-Arm begünstigender Trend wurde in der hormonrezeptor-positiven Population beobachtet, bei denen der Abschluss der Trastuzumab-Therapie weniger als ein Jahr zurücklag [HR 0,79 (95% KI, 0,55, 1,13)].
|



